2026-04-15
临影医药作为专业独立影像评估(IRC)服务商,可为放射性药物提供符合FDA/NMPA 影像评估要求的全流程 IRC 支持,涵盖辐射剂量评估、安全性监测、影像终点评估、数据质控与注册申报影像资料合规支持,助力临床试验顺利通过注册核查。
一、监管趋势:核药影像数据合规要求全面升级
近年来,全球监管机构对放射性药物的研发、临床应用与上市申报日趋规范,尤其对辐射剂量、辐射安全、器官毒性、长期风险等方面提出明确且严格的要求。无论是 FDA、EMA 还是 NMPA,均将辐射剂量评估数据列为核药申报影像资料的必备内容。缺乏完整、规范、可信的剂量学与安全性影像数据,将直接导致申报失败或发补。
在这一背景下,独立影像评估(IRC)作为独立第三方评估机构,其提供的标准化影像与剂量评估数据,已成为核药合规申报的重要保障。
二、审评核心:辐射剂量安全性与临床疗效评估
放射性药物的审批核心是“获益-风险比”:疗效获益必须显著大于辐射相关风险。监管机构重点关注以下问题:
•人体器官吸收剂量是否在可接受安全范围?
•剂量限制性器官是哪些?
•最大耐受剂量是多少?
•给药方案是否合理?
•长期辐射暴露是否增加继发肿瘤风险?
这些问题的答案,几乎全部依赖于医学影像定量与剂量学研究。若影像数据由各中心自行评估,缺乏统一标准与独立复核,审评机构通常不予认可。
三、监管对核药影像数据的三大核心要求
监管机构对核药临床试验影像数据管理的核心要求可概括为三点:
IRC 通过中心化管理、盲态评估、质量控制、电子数据留存,天然满足这三大要求,因此被监管机构广泛接受和推荐。
四、注册申报影像资料要求
在注册申报影像资料要求中,与辐射剂量相关的影像部分通常包括:
1.影像评估方案
2.采集 SOP
3.定量方法学
4.器官剂量估算结果
5.辐射安全性评价
6.疗效影像终点数据(ORR、rPFS、DOR)
7.独立影像评估报告(IRC Report)
任何一个环节缺失或不规范,都可能引发发补意见,延长上市周期。尤其在以影像学终点(肿瘤客观缓解率(ORR)、影像学无进展生存期(rPFS)、缓解持续时间(DOR))为主要疗效终点的核药临床试验影像评估中,IRC 报告是审评重点核查内容。
五、临影医药:核药全链条 IRC 支持
临影医药可从监管合规角度为放射性药物提供全链条独立影像评估服务:
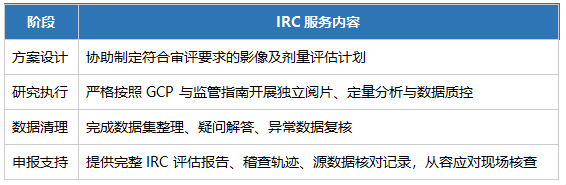
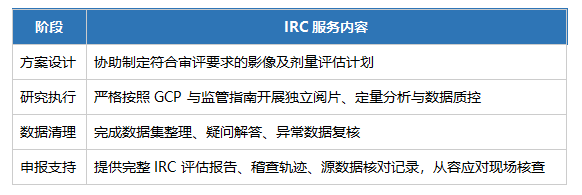
临影凭借在核药 IRC 领域的经验,可帮助申办方提前规避合规风险,减少发补,加速上市进程。
六、展望:IRC 在核药合规申报中的地位将更加关键
随着核药赛道持续火热,监管要求将不断细化升级,独立影像评估(IRC)在合规申报中的地位将更加关键。只有建立科学、规范、独立的影像评估体系,才能真正实现核药研发高质量发展,为患者提供安全有效的创新治疗方案。
Q&A
Q1:监管机构审评核药时重点关注辐射相关哪些内容?
答:重点关注器官吸收剂量、安全阈值、剂量限制性毒性、给药方案合理性与长期风险。
Q2:监管对核药影像数据的三大核心要求是什么?
答:标准化(统一 SOP)、可追溯(完整痕迹)、可重复(高度一致)。
Q3:为什么监管机构更认可 IRC 提供的影像数据?
答:IRC 独立、盲态、标准统一,数据更客观、可靠、可稽查。
Q4:核药申报中缺少 IRC 影像评估会有什么风险?
答:可能被审评发补、数据不被认可,甚至导致申报注册失败。
Q5:核药临床试验中 IRC 的核心影像终点指标有哪些?
答:主要包括肿瘤客观缓解率(ORR)、影像学无进展生存期(rPFS)、缓解持续时间(DOR)。
Q6:临影如何支持核药满足监管合规要求?
答:提供符合 GCP 的 IRC 评估、全流程影像阅片与定量分析、完整数据痕迹、影像终点评估报告及核查支撑资料。
Q7:IRC 与本地阅片在核药申报中的差异?
答:本地阅片由各研究中心独立完成,标准不统一、数据可追溯性不足;独立影像核查(BICR)由第三方团队统一标准、集中阅片,数据可稽查、可追溯,更符合监管机构审评要求。