2026-03-25
有临来雅

抗肿瘤药物I期临床试验是连接实验室研究与临床应用的关键桥梁。作为一家深耕临床试验统计设计的专业数统服务公司,有临来雅团队在服务众多创新药企的过程中发现,如何在保障受试者安全的前提下,快速、准确地找到最大耐受剂量(MTD),往往是研发团队面临的首要难题。
长期以来,传统的“3+3”设计因其操作简单而被广泛使用,但其固有的缺陷——如MTD估算不准、受试者暴露于过量毒性风险——也日益凸显。随着创新药研发的提速,一种名为BOIN(Bayesian Optimal Interval)的设计方法正逐渐成为行业新趋势。
一、 为什么BOIN设计被称为“最优”解?
BOIN设计全称为贝叶斯最优区间设计,由美国MD Anderson癌症中心袁鹰教授团队于2015年提出,并于2021年获得FDA Fit-For-Purpose认证。
不同于传统设计的死板,BOIN设计的核心在于“最优区间”概念。其思路非常直观:通过最小化将受试者分配至不恰当剂量(过高或过低)的概率,来确定决策边界。简单来说,它设定了两个阈值(λe和λd),将DLT发生率划分为三个区域(如表1):
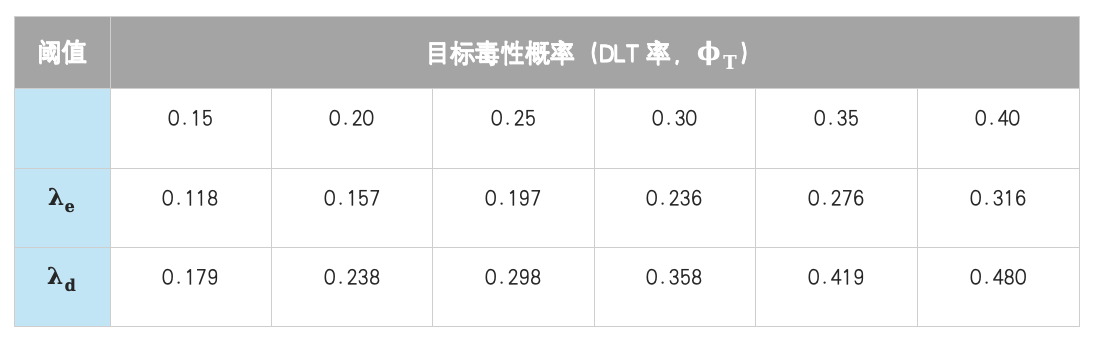
表1:BOIN 设计的剂量升降阈值
二、 实际应用场景:决策透明,沟通高效
想象这样一个场景:在一个抗肿瘤新药的I期剂量递增会议上,医学团队与统计师正在讨论下一队列的入组剂量。使用复杂的模型设计(如CRM)时,临床医生往往难以理解背后的统计逻辑,导致决策效率低下。
而采用BOIN设计,统计师可以在试验开始前就生成一张清晰的“决策表”。
例如,设定目标毒性概率ϕ=0.3,队列大小为3。研究者只需看表:如果当前剂量组3例受试者中出现0例DLT,查表可知决策为“递增”;若出现2例DLT,决策为“递减”。这种“所见即所得”的决策方式,极大地降低了沟通成本,让临床医生能更专注于受试者的医学判断,而非陷入复杂的统计计算泥潭。
三、 监管认可与落地工具
BOIN设计的优势不仅在于操作简便,更在于其统计效能优良。研究表明,其识别MTD的准确率显著优于“3+3”设计,且能有效保护受试者免受过高毒性的伤害。
监管机构方面,FDA已有多项基于BOIN设计的临床试验获批;CDE在2020年发布的《抗肿瘤药物临床试验统计学设计指导原则(试行)》中也明确点名认可,称其“易于实施,具有与基于模型的设计相当的性能”。
在落地执行层面,BOIN设计也极其友好。除了R语言程序包,研发团队还可通过 http://www.trialdesign.cn 等可视化平台,无需编写代码,一键生成决策表格和模拟报告,大幅缩短了方案设计周期。
结语
从“基于规则”到“模型辅助”,BOIN设计代表了I期临床试验设计的进化方向。它保留了传统设计的简便性,同时具备了模型设计的统计优良性。对于追求研发效率与质量的创新药企而言,掌握并应用BOIN设计,或许是优化临床开发策略的重要一步。
参考文献:
[1] Yuan Y, Hess K R, Hilsenbeck S G, et al. Bayesian Optimal Interval Design: A Simple and Well-Performing Design for Phase I Oncology Trials[J]. Clinical Cancer Research, 2016, 22(17):4291.
[2] Liu S, Yuan Y. Bayesian optimal interval designs for phase I clinical trials[J]. Journal of the Royal Statistical Society: Series C (Applied Statistics), 2015, 64.
[3] 国家药品监督管理局. 抗肿瘤药物临床试验统计学设计指导原则(试行)[S]. 2020.